
01、研究背景
随着工业化和城市化的加剧,空气污染已成为全球最紧迫的环境健康挑战之一越来越多的研究表明,PM2.5、NO₂、SO₂、O₃、VOCs等可以通过氧化应激等来干扰免疫稳态,空气污染驱动的免疫调节失常与各种慢性炎症和自身免疫性疾病的发生机制有关
而在免疫介导的疾病中,银屑病是一种典型的慢性炎症性皮肤病,最近的流行病学研究表明,长期暴露于空气污染物与银屑病的发病率和严重程度增加有关 , 但目前缺乏机制解释。空气污染是否通过影响免疫相关分子和通路,参与银屑病的发生与进展?
02、研究方法
1.从公共数据库编译银屑病相关和污染物相关基因,取其交集。
2.对交集基因进行网络毒理学分析(包括蛋白质蛋白质相互作用和通路富集)。
3.利用五个GEO转录组数据集构建113个机器学习分类器,以确定一个稳健的诊断基因特征。
4.用“scTenifoldKnk” R包对病变银屑病单细胞数据集中角质形成细胞亚群进行了虚拟敲除
5.体外和体内验证S100A9在银屑病模型中的应用
4.使用该基因特征,对七种结构明确的污染物与免疫基因靶点进行下游分子对接模拟。
03、研究结果
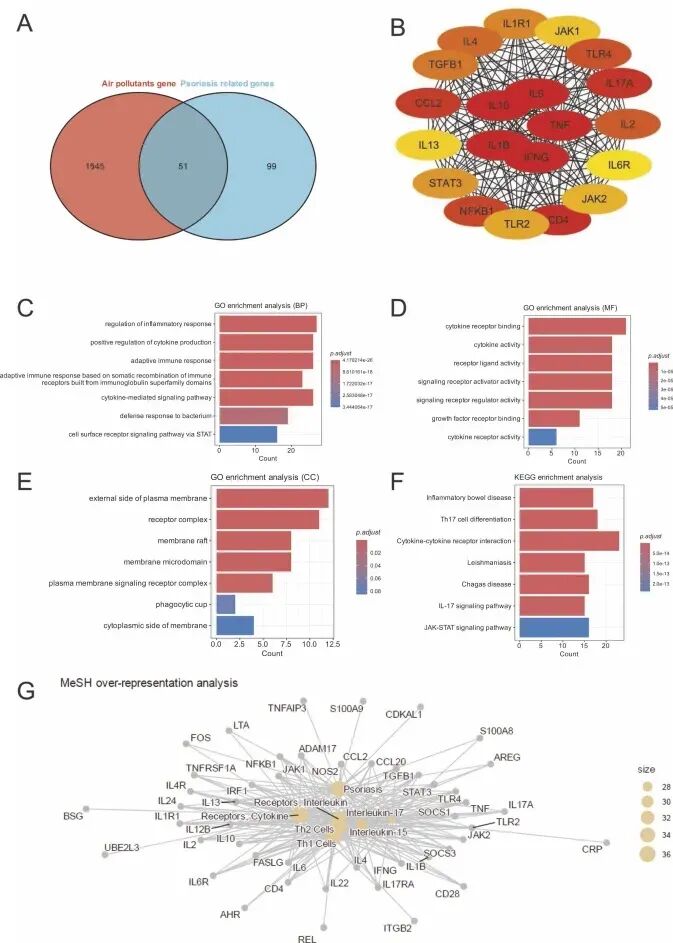
1.空气污染物相关基因与银屑病相关基因获取
在CTD(Comparative Toxicogenomics Database)数据库检索到与选定空气污染物相关的1596个人类基因
在GeneCards、OMIM、GWAS Catalog、MalaCards、Open Targets 5个数据库中提取150个与银屑病相关的基因

2.污染物与银屑病交集基因鉴定
将空气污染物相关基因与银屑病相关基因取交集得到 51 个共同基因,并用 STRING 构建 51 个基因的 PPI 网络,去除未连接的节点后剩余45个基因。使用Cytoscape和MCC算法进行拓扑分析筛选出几个免疫相关:TNF、IL6、IL1B、IFNG、JAK1、STAT3。KEGG结果显示这些基因涉及免疫、炎症等机制,显著富集在JAK-STAT和IL-17信号通路。说明它们在介导空气污染物引起的银屑病免疫激活中有潜在作用
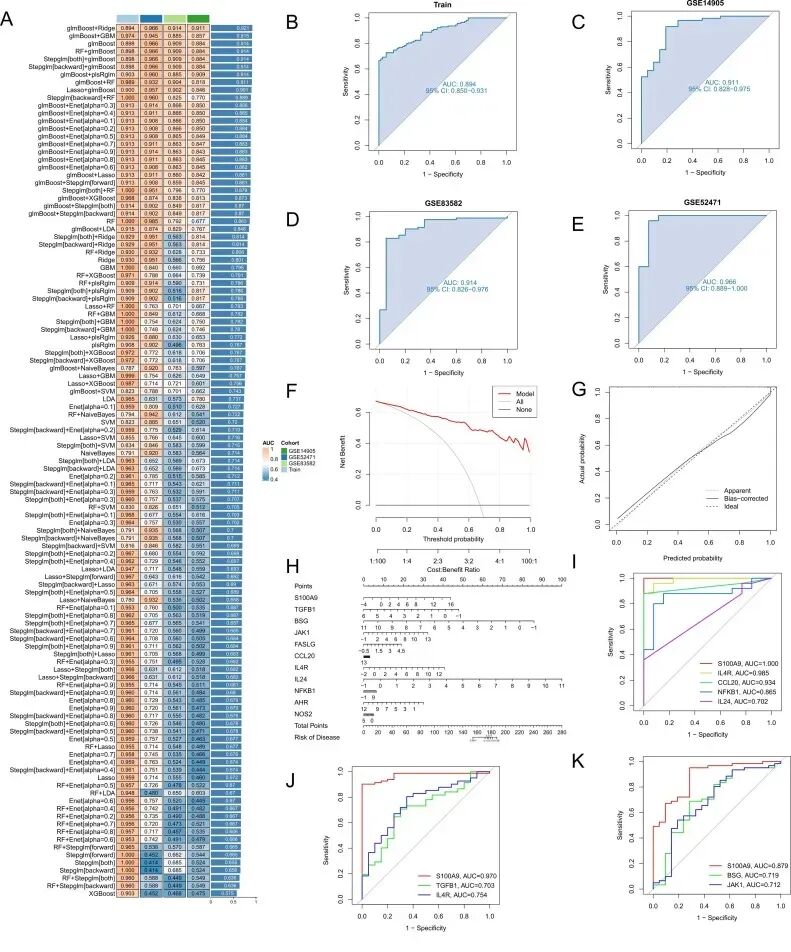
3.基于机器学习的关键诊断基因识别和模型开发
用12 种机器学习算法构建113个预测模型,得到其中最优模型,该模型包含12 个关键基因特征:IFNG、S100A9、JAK1、CCL20、IL4R、TGFB1 等。
并在三个独立队列(GSE14905、GSE83582 和 GSE52471)中进行了稳健的外部验证,AUC 分别为 0.911、0.914 和 0.966。
S100A9 在多个模型中权重最高,凸显其核心地位
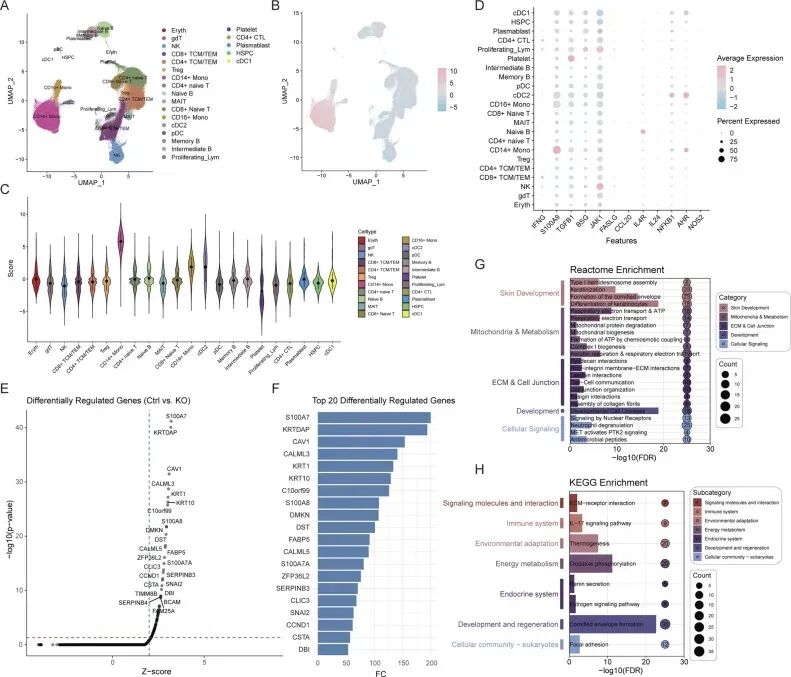
4.单细胞分析和虚拟细胞敲除
S100A9在PBMC的CD14⁺ 单核细胞细胞和角质形成细胞、髓系细胞中高表达
暗示其在“免疫-表皮互作”中的作用
接着使用 scTenifoldKnk在单细胞层面模拟敲除 S100A9
发现差异基因富集于:表皮角化和分化、IL-17 相关炎症通路、线粒体代谢与氧化磷酸化,证明S100A9参与调控表皮异常与炎症
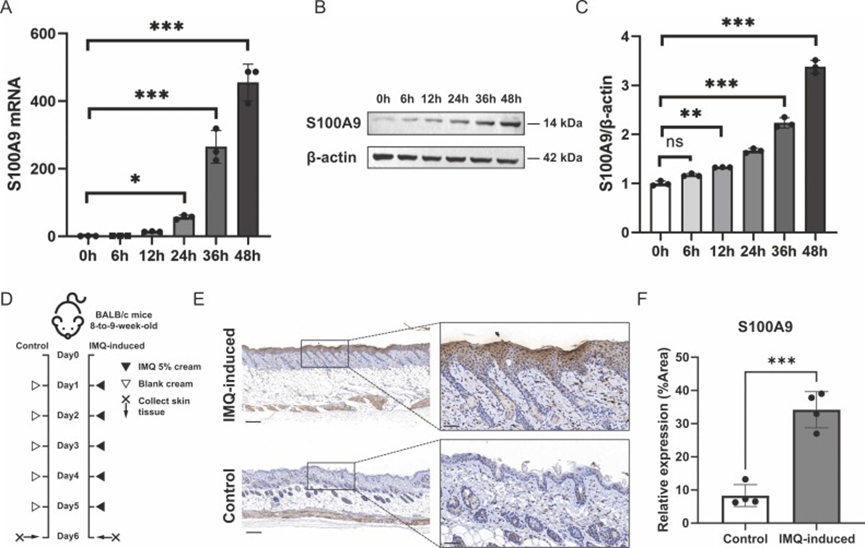
5.体外和体内验证S100A9在银屑病模型中的应用
进行体外实验来验证IL-17影响S100A9的作用IL-17 刺激 HaCaT 细胞,结果显示,IL-17处理显著上调了S100A9的mRNA和蛋白水平 。并建立了IMQ诱导的小鼠银屑病样模型,发现S100A9 在银屑病中显著上调,可能在该病的发病机制中作为一个潜在的风险因素,从而进一步验证了机器学习模型的可靠性。
6.分子对接揭示污染物-蛋白质相互作用
对7种空气污染物与12个银屑病相关靶点进行分子对接
其中甲苯与 AHR、JAK1、NOS2 结合能较强

04、总结
这项研究通过网络毒理学、机器学习、分子对接等方法,将空气污染物暴露、免疫基因激活和银屑病联系起来,揭示了空气污染与银屑病的作用机制,筛选出12个相关靶点,其中S100A9 可能是连接环境暴露与免疫的关键分子。甲苯与AHR、JAK1、NOS2具有较强的相互作用
转载自CSDN-专业IT技术社区



